لا يوجد علاج نهائي متاح على نطاقٍ واسع حتى الآن، لكن هناك تقدّم حقيقي في عدة محاور — خصوصاً: (1) الأجسام المناعية واسعة التحييد (bNAbs) كمزيج علاجي/وقائي، (2) تحرير الجينات (CRISPR/CCR5) لتكوين خلايا مقاومة، (3) مناهج استهداف المُخزن الفيروسي (LRAs، «shock & kill» و«block & lock»)، و(4) مناعيات خلوية متقدمة مثل CAR-T. كلٌّ منها واعد لكن ما زالت المرحلة التجريبية أو محدودة التطبيق.
النهج الكبرى حالياً — ما هي وماذا حققت حتى الآن
أ. الأجسام المناعية واسعة التحّييد (bNAbs)
-
الفكرة: استخدام أجسام مناعية مُهندَسة (mAbs) تحيّد نطاقًا واسعًا من سلالات HIV. تُعطى منفردة أو كمجموعات (cocktails) لتعزيز التغطية ومنع مقاومة الفيروس.
-
ما تحقق: تجارب أظهرت كبتًا مؤقتاً للحمل الفيروسي وإطالة الزمن حتى الارتداد عند إيقاف الـART؛ تجارب حديثة أشارت إلى أن مزيج ثلاثي من bNAbs يعطي تغطية أفضل ويقلّل فرصة هروب الفيروس. لكن الفعالية تعتمد على حساسية فيروس المجتمع لهذه الأجسام. Nature+1
ب. تحرير الجينات (CRISPR وغيرها) — إستراتيجيّات مقاومة الخلايا
-
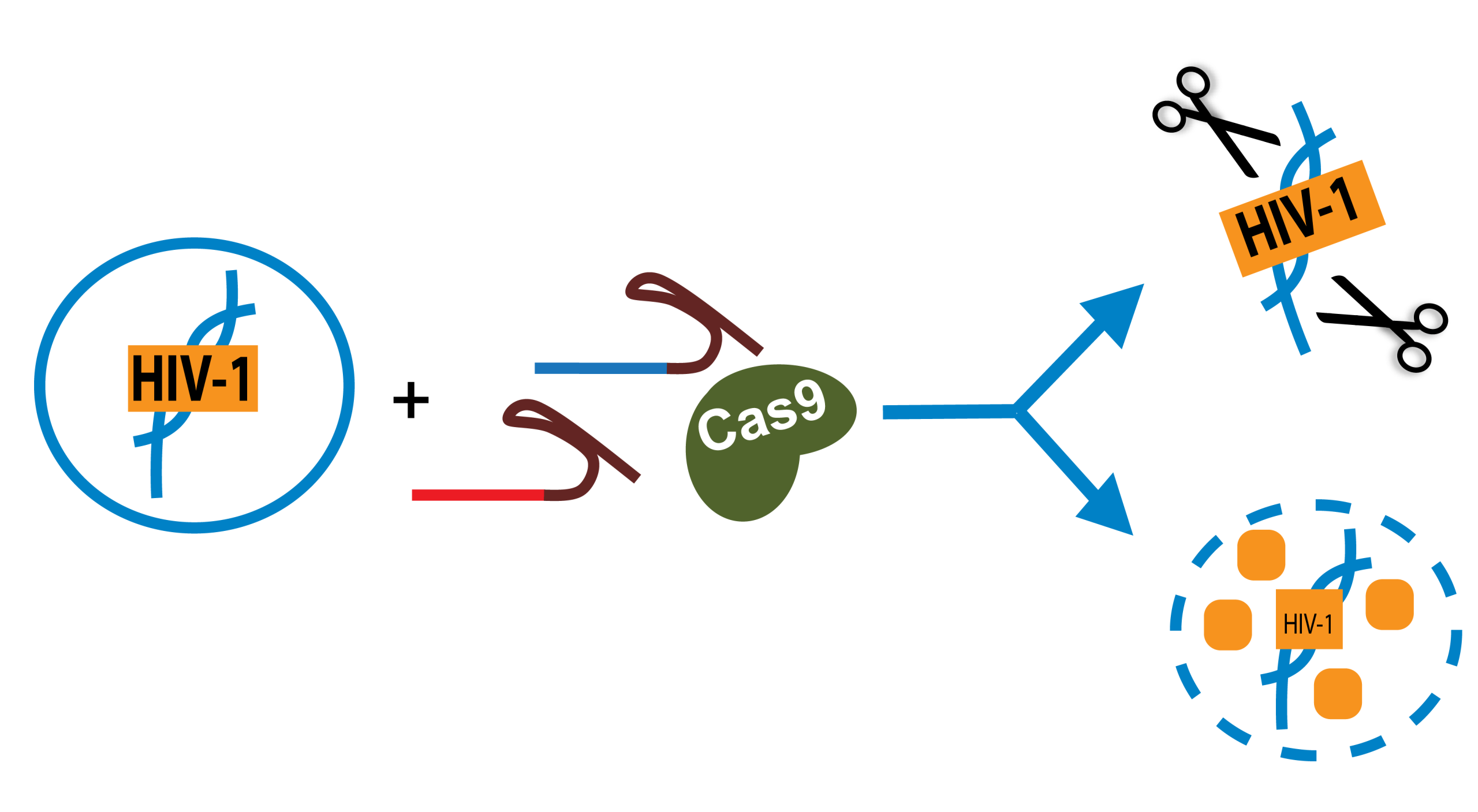
الفكرة: تعديل خلايا جذعية أو خلايا مناعية لإزالة مستقبلات الدخول (مثل CCR5) أو استئصال حمض نووي لفايروسي داخل الخلايا.
-
إنجازات مهمة: تجارب أولية في البشر (أول تجارب CRISPR المبلّغة في 2024–2025) أظهرت استهدافًا مقصودًا للـDNA، ونتائج آمنة أولية — لكن التحديات تتضمن كفاءة التوصيل، الشواذ الخارجي (off-target) والقدرة على الوصول لكل الخلايا المصابة. EATG+1
ج. استهداف المخزّن (Latency reversing agents — LRAs; “shock & kill”)
-
الفكرة: إيقاظ الفيروس الخامل داخل خلايا الذاكرة ثم قتله أو تطهيره بواسطة الجهاز المناعي.
-
الوضع الحالي: هناك LRAs متعددة اختُبرت سريريًا (مثلاً romidepsin، panobinostat وغيرها) وأظهرت قدرة على إعادة تنشيط الفيروس، لكن النتيجة العملية على تقليل المخزون الفيروسي الدائم محدودة حتى الآن، وغالبًا تحتاج إلى تكامل مع مناهج مناعية أخرى. PMC+1
د. مناعيات خلوية متقدمة (CAR-T، T-cell therapies)
-
الفكرة: هندسة خلايا T لمهاجمة الخلايا الحاملة لفيروس HIV.
-
التقدّم: دراسات ما قبل السريرية وسلسلة تجارب مبكرة أظهرت فعالية في تقليل الخلايا الحاملة في بعض حالات، وهناك تطورات في تحسين ثبات الاستهداف وتقليل السميّة. لكن التكلفة والسمّيات والحاجة لتعديل فردي تبقيها محدودة سريريًا الآن. PMC
هـ. زراعة نخاع/حالات شفاء استثنائية (Berlin / London patients)
-
دروسها: زرع خلايا جذعية ذات طفرة CCR5-Δ32 نتج عنه شفاء في حالات نادرة؛ هذه الحالة عملية خطيرة وغير قابلة للتكرار كعلاج شعبي، لكنها أكدت قابلية الشفاء عبر استبدال خلايا مستضيفة بمقاومة وراثية. PMC
أبرز النتائج والدراسات الحديثة (مفصّلة وباختصار)
-
تركيبات ثلاثية من bNAbs أظهرت تغطية أفضل ونتائج سريرية واعدة (تقليل هروب الفيروس وإطالة فترات السيطرة بعد إيقاف العلاج). هذا ظهر في دراسات منشورة عامي 2024–2025. Nature+1
-
أول تجارب بشرية لـCRISPR مبلّغة عام 2024–2025 أظهرت إمكانية استهداف الحمض النووي الفيروسي أو مواقع دخول الفيروس مع نتائج أمان أولية؛ العمل مستمر لرفع الكفاءة وتقليل التأثيرات غير المقصودة. EATG+1
-
التوليفات العلاجية (مزيج bNAbs + مناهج مناعية + LRAs) باتت الاتجاه الأوضح — أن نهجًا وحيدًا نادرًا ما يكفي؛ الأبحاث الآن تجرّب بروتوكولات متعدّدة الخطوات. ScienceDirect
-
أبحاث ناقلات الجين (AAV) لتوصيل bNAbs أو CRISPR في الجسم) أظهرت إمكانية إعطاء حماية طويلة الأمد لكن تحتاج تقييمًا طويل المدى للسلامة. Nature
أهم العقبات العلمية والعملية
-
مخزون الفيروس الخامل (reservoir) موزّع في أنسجة متعددة ويصعب الوصول إليه.
-
تنوع الفيروس: اختلاف السلالات يجعل أي علاج استهدافي عرضة لهروبٍ فيروسي.
-
السلامة والسمّيات: تحرير الجينات والتعديلات المناعية تحمل مخاطراً (off-target effects، استجابة مناعية غير مرغوبة).
-
قابلية التنفيذ والوصول: بعض العلاجات (زراعة نخاع/CAR-T) مكلفة ومعقّدة وغير قابلة للتوسيع عالمياً.
-
قيود الترجمة من حيواني إلى إنسان — فعالية في المختبر لا تساوي بالضرورة فائدة سريرية كبيرة. PMC+1
ماذا يعني هذا للمرضى والعامّة الآن؟
-
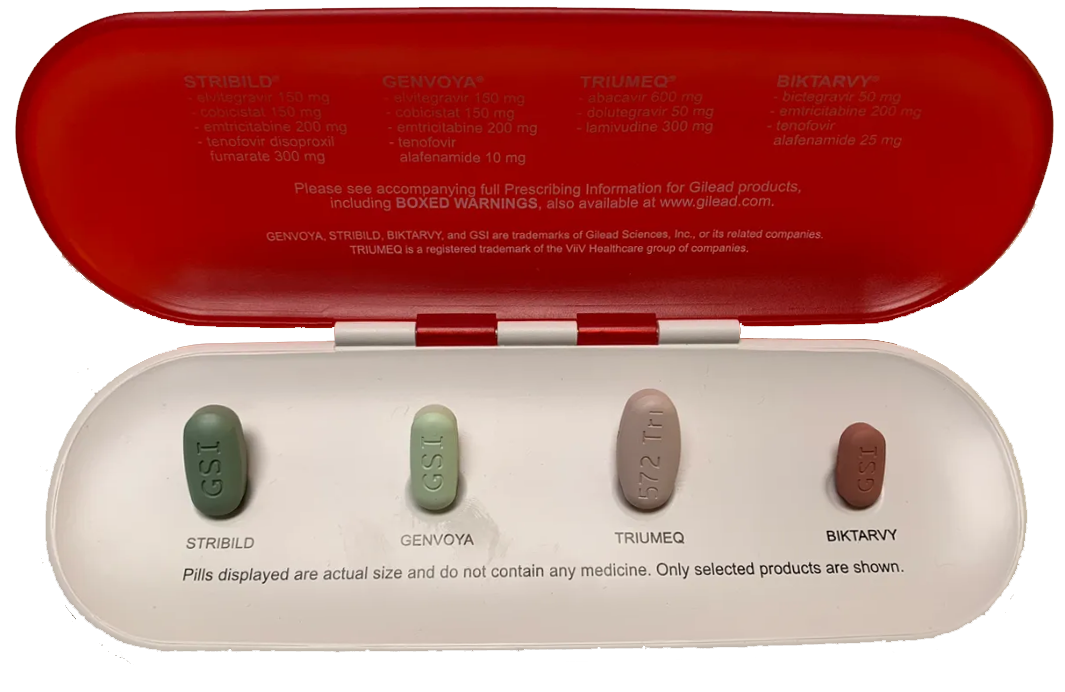
لا تزال التوصية الأساسية: الالتزام بالعلاج المضاد للفيروسات (ART) — لأن ART تمنع تطور المرض، تحسن الحياة، وتحوّل المرضى إلى غير ناقلين جنسيًا إذا كان الحمل الفيروسي غير قابل للكشف (U=U). أي أمل علاجي لا يلغِي هذا. Nature
-
اعتبار الأبحاث الحالية أمناً متقدماً لكن تجريبياً — المرضى يجب أن يستشيروا الفرق الطبية عند التفكير في الانخراط في تجارب سريرية.
-
تحذير من الممارسات غير المثبتة تجاريًا: تجنّب “علاجات معجزة” أو تجارب خارج المؤسّسات الأكاديمية؛ قد تكون خطرة.
مراجع
-
مراجعات شاملة عن bNAbs ونتائج تجارب (2024–2025). PMC+1
-
دراسة Nature (2024) عن مزيج ثلاثي من bNAbs — دليل على تحسّن التغطية. Nature
-
ملخصات ومتابعات أولية لتجارب CRISPR في الإنسان (2024–2025). EATG+1
-
مراجعات ومقالات عن LRAs ووضع “shock & kill” و«block & lock». PMC+1
-
مراجعات عامة عن ابتكارات الجينات والعرقلة أمام الترجمة إلى علاج شامل. PMC